1.4 Lo stato gassoso
QUIZ 4
Ad un palloncino contenente 1,0 moli di elio gas a 25 °C vengono aggiunte altre 3,0 moli di elio. Se la temperatura resta costante e il volume del palloncino raddoppia, come sarà modificata la pressione rispetto a quella originale all’interno dello stesso palloncino?
Applichiamo la legge dei gas perfetti:
P · V = n · R · T
Nella condizione iniziale abbiamo: n1 =1 mol, T1(25+273 K) eV1 . La pressione vale perciò:
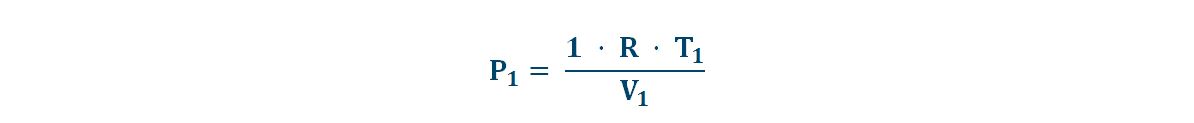
Nella nuova condizione abbiamo aggiunto tre moli alla mole già presente n2=4 mol, la temperatura invariata al valore T1 ed il volume raddoppiato al valore 2·V1. La pressione vale perciò:
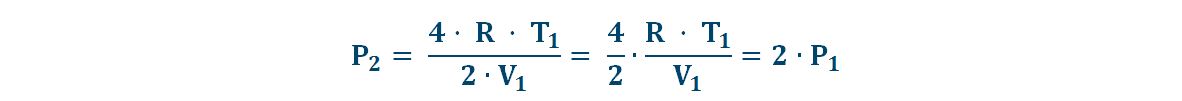
La pressione è raddoppiata.
Potremmo anche ragionare, in modo più intuitivo così:
In base alla legge dei gas perfetti, se la temperatura rimane costante, la pressione è direttamente proporzionale al numero di moli e inversamente proporzionale al volume:

Ricaviamo il nuovo valore della pressione sapendo che il numero di moli quadruplica e il volume raddoppia:
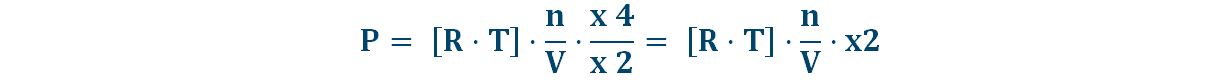
Il valore della pressione subisce un fattore di proporzionalità moltiplicandosi per 2.
QUIZ sullo stato gassoso |
|||
|---|---|---|---|
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito


