9.3 Acidi e basi Definizioni
QUIZ 19
Veterinaria 2015
Tutte le equazioni sottostanti descrivono reazioni acido-base. In quale delle reazioni il composto sottolineato si comporta da acido di Lewis e non da acido di Brønsted-Lowry?
La definizione di acido e di base secondo Lewis è stata introdotta per poter classificare come acidi e basi sostanze che non possiedono idrogeno ma che reagiscono con uno scambio di una coppia di elettroni come la reazione tra ammoniaca NH3 e fluoruro di boro BF3 che reagiscono come in figura.
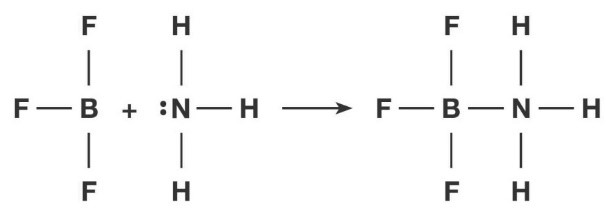 |
L’ammoniaca, comportandosi da base, dona il suo doppietto libero al fluoruro di boro che si comporta da acido.
In tutte le altre reazioni presenti nelle altre risposte c'è una sostanza che cede un H+ ed un'altra che lo riceve. Per questo motivo sono classificabili come acidi e basi secondo Brønsted e Lowry.
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito


